【生醫評析】量身打造以AI技術為基礎之醫療器材軟體上市法規環境~美國FDA公布新管理架構概念討論文件
2019-06-11 孫世昌 資深顧問
「人工智慧演算法」(Artificial Intelligence Algorithms)是一種可藉其於真實世界使用過程中所收集到之數據資料持續進行學習並採取相對應行動之一種「軟體」;而隨著此類技術之逐漸成熟,廠商已開始將其應用,轉而擴及至醫療照護領域,以協助臨床醫師早期篩檢疾病及提供合適治療上建議。以美國為例,單於去(2018)年間,FDA已分別核准了兩項以AI軟體為基礎之醫療器材產品上市,其中之一,是一種利用AI軟體來協助檢測「糖尿病視網膜病變」(Diabetic Retinopathy,可導致喪失視力之眼部疾病)之醫療器材;而另一,則是一種利用AI軟體來預先警示專業醫療服務提供者,該病患是否具潛在中風危險之醫療器材(屬臨床決策輔助)。為確保利用先進AI演算法所開發出創新醫療器材產品之安全性與功效、回應相關業者對法規管理面需求,FDA於今(2019)年4月2日時,正式對外發出聲明,將針對此類利用「人工智慧」或「機器學習」(Machine Learning,簡稱ML)技術所開發出之醫療器材,特別量身制訂一套新的法規管理架構,並同時公布由FDA方面所預先構思出之新法規管理架構概念「討論文件」(Proposed Discussion Paper),供外界先行參考與廣泛收集相關專家及業者之回饋意見,以作為FDA後續草擬新法規管理架構時之重要參考基礎。
有關FDA此次為針對以AI/ML為基礎所開發之新醫療器材產品量身制訂一套新法規管理架構此目的所先行公布之「針對做為醫療器材使用之以AI/ML為基礎軟體之法規管理架構修正草案-討論文件」(Proposed Regulatory Framework for Modifications to Artificial Intelligence/Machine Learning (AI/ML)-Based Software as a Medical Device (SaMD)-Discussion Paper),其內容重點臚列如下:
(一)說明以AI與ML為基礎之技術,具有可藉每日所提供健康照護服務過程中所產生之大量數據資料中獲得新的、重要的Insight,來改善健康照護服務之潛力,其高附加價值之應用,包括:疾病早期檢測、更精準的診斷、新病徵或人體生理模式鑑別、及促進個人化診斷/醫療發展。
(二)點出以上述AI/ML技術所開出之軟體,因具持續學習並不斷改善其性能(適應)之能力,使得其特別適合作為一種醫療器材產品使用,而換個角度來說,當此類以AI / ML為基礎之軟體,欲作為治療、診斷、治癒、緩解或預防疾病目的使用時,即成為受FD&CA所規範之醫療器材,並被FDA與國際法規主管機關論壇(International Medical Device Regulators Forum,簡稱IMDRF) 稱為「軟體即醫療器材」(Software as a Medical Device,以下簡稱SaMD)。
(三)於文件中強調,FDA將嘗試透過適當修訂法規管理方式,讓上述以AI/ML為基礎之醫療器材軟體,在仍能維持其本身之安全性與有效性等前提下,充分發揮其功能,並藉此改善病患所獲得之醫療照護服務品質。
(四)按討論文件內容,就以AI/ML為基礎SaMD之軟體修改(Modification),依其對使用者(包括:病患、專業醫療照護人員或其他人)所可能造成之影響,區分為如下幾種修改類型:
有關FDA此次為針對以AI/ML為基礎所開發之新醫療器材產品量身制訂一套新法規管理架構此目的所先行公布之「針對做為醫療器材使用之以AI/ML為基礎軟體之法規管理架構修正草案-討論文件」(Proposed Regulatory Framework for Modifications to Artificial Intelligence/Machine Learning (AI/ML)-Based Software as a Medical Device (SaMD)-Discussion Paper),其內容重點臚列如下:
(一)說明以AI與ML為基礎之技術,具有可藉每日所提供健康照護服務過程中所產生之大量數據資料中獲得新的、重要的Insight,來改善健康照護服務之潛力,其高附加價值之應用,包括:疾病早期檢測、更精準的診斷、新病徵或人體生理模式鑑別、及促進個人化診斷/醫療發展。
(二)點出以上述AI/ML技術所開出之軟體,因具持續學習並不斷改善其性能(適應)之能力,使得其特別適合作為一種醫療器材產品使用,而換個角度來說,當此類以AI / ML為基礎之軟體,欲作為治療、診斷、治癒、緩解或預防疾病目的使用時,即成為受FD&CA所規範之醫療器材,並被FDA與國際法規主管機關論壇(International Medical Device Regulators Forum,簡稱IMDRF) 稱為「軟體即醫療器材」(Software as a Medical Device,以下簡稱SaMD)。
(三)於文件中強調,FDA將嘗試透過適當修訂法規管理方式,讓上述以AI/ML為基礎之醫療器材軟體,在仍能維持其本身之安全性與有效性等前提下,充分發揮其功能,並藉此改善病患所獲得之醫療照護服務品質。
(四)按討論文件內容,就以AI/ML為基礎SaMD之軟體修改(Modification),依其對使用者(包括:病患、專業醫療照護人員或其他人)所可能造成之影響,區分為如下幾種修改類型:
1. 與功能表現相關之修改(但不改變原預期用途或新的輸入資料類型):
此種修改類型,可改進軟體之臨床分析及功能表現(包括以相同種類輸入資料之AI/ML架構變更),而針對此修改類型,製造商通常聚焦在「於不改變所聲稱該產品原預期用情況下,為使用者升級新的功能表現(例如:於數位乳房X光造影檢測可疑之病灶時,增加 SaMD之敏感度)。
2. 與輸入資料類型相關之修改(但不改變原預期用途):
此種修改類型,是改變AI/ML演算法所使用之輸入資料,目的可能是為了使用新類型之輸入資料而對演算法所進行之變更,且無涉及改變該產品原預期用途,其案例包括:
(1)擴大 SaMD與其他來源之相同類型輸入資料間之相容性(例如:修改SaMD以支援與由其他製造商所生產之CT掃描儀之相容性);或
(2)增加不同類型之輸入資料(例如:擴大某種可用以診斷心房顫動SaMD 之輸入資料類型,來涵蓋與血氧檢測有關之輸入資料)。
(1)擴大 SaMD與其他來源之相同類型輸入資料間之相容性(例如:修改SaMD以支援與由其他製造商所生產之CT掃描儀之相容性);或
(2)增加不同類型之輸入資料(例如:擴大某種可用以診斷心房顫動SaMD 之輸入資料類型,來涵蓋與血氧檢測有關之輸入資料)。
3. 與 SaMD預期用途有關之修改:
SaMD所提供資料之臨床重要性發生改變之修改(例如:其信心數值從「診斷輔助」(驅動臨床管理)轉變成「明確診斷」)。另外,此類修改還可能包括可導致原本適用之醫療照護狀況或生理條件狀態發生改變之修改,例如:
(1)擴大原預期病患群體(例如:將原適用於18歲或以上成年人之 SaMD,經修改,後可進一步適用於兒童病患群體);或
(2)擴大原預期適用之疾病或生理條件(例如:擴大用於檢測某種癌症之SaMD演算法,可用於進行另一種癌症病灶之檢測)。
(1)擴大原預期病患群體(例如:將原適用於18歲或以上成年人之 SaMD,經修改,後可進一步適用於兒童病患群體);或
(2)擴大原預期適用之疾病或生理條件(例如:擴大用於檢測某種癌症之SaMD演算法,可用於進行另一種癌症病灶之檢測)。
(五)依本項討論文件內容,因此類新興軟體具備可在真實世界中使用過程中進行自我學習,與不斷改進、適應之能力,故於文件中點出,對以AI/ML為基礎之 SaMD產品之上市管理,將於新管理架構中導入「整體產品生命週期法規管控」(Total Product Lifecycle Control,簡稱TPLC)概念(亦即自產品上市前開發階段至上市後之功能表現持續進行評估及監控)(如圖一)。
在TPLC概念下,FDA擬採取之一般性管理原則如下:
1. 將要求製造商就此類新興軟體產品建立可符合相應標準及相關法規之「品質管理系統」(Quality Systems)及遵循「優良機器學習規範」(Good Machine Learning Practices,簡稱GMLP)。
2. 針對須提交上市申請之SaMD,執行上市前審查,以確保此類新興軟體產品之安全性與功效,並將為製造商建立明確之法規要求,以持續於產品整體生命週期中,妥善管理其對病患(或使用者)所具之潛在風險。
3. 製造商應就其所開發之AI/ML醫療器材產品進行監控,並應採納以風險為基礎之管理方法、及其他於“Deciding When to Submit a 510(k) for a Software Change to an Existing Device”指引文件中所描述之相關方式,例如:SaMD預定規格(SaMD Pre-Specifications,簡稱SPS)、及演算法變更協定(Algorithm Change Protocol,簡稱ACP)。
4. 利用持續更新並提交產品上市後「於真實世界使用之功能表現監控報告」(Real-World Performance Monitoring Report)或援引其他既有之相關機制,以增加此類產品對使用者及FDA之透明度。針對上開概念性管理架構,FDA局長 Scott Gottlieb M.D.於其官方聲明中補充:「我們還有許多的工作要做,以持續建構此一初步之概念構想,而同時,我們十分希望能仰賴來自專家與各利益相關者所提出之評論與回饋意見,以協助我們繼續思考如何妥善運用AI來改善病患醫療照護技術與服務」。
2. 針對須提交上市申請之SaMD,執行上市前審查,以確保此類新興軟體產品之安全性與功效,並將為製造商建立明確之法規要求,以持續於產品整體生命週期中,妥善管理其對病患(或使用者)所具之潛在風險。
3. 製造商應就其所開發之AI/ML醫療器材產品進行監控,並應採納以風險為基礎之管理方法、及其他於“Deciding When to Submit a 510(k) for a Software Change to an Existing Device”指引文件中所描述之相關方式,例如:SaMD預定規格(SaMD Pre-Specifications,簡稱SPS)、及演算法變更協定(Algorithm Change Protocol,簡稱ACP)。
4. 利用持續更新並提交產品上市後「於真實世界使用之功能表現監控報告」(Real-World Performance Monitoring Report)或援引其他既有之相關機制,以增加此類產品對使用者及FDA之透明度。針對上開概念性管理架構,FDA局長 Scott Gottlieb M.D.於其官方聲明中補充:「我們還有許多的工作要做,以持續建構此一初步之概念構想,而同時,我們十分希望能仰賴來自專家與各利益相關者所提出之評論與回饋意見,以協助我們繼續思考如何妥善運用AI來改善病患醫療照護技術與服務」。
圖一、嵌入FDA所提之TPLC概念圖
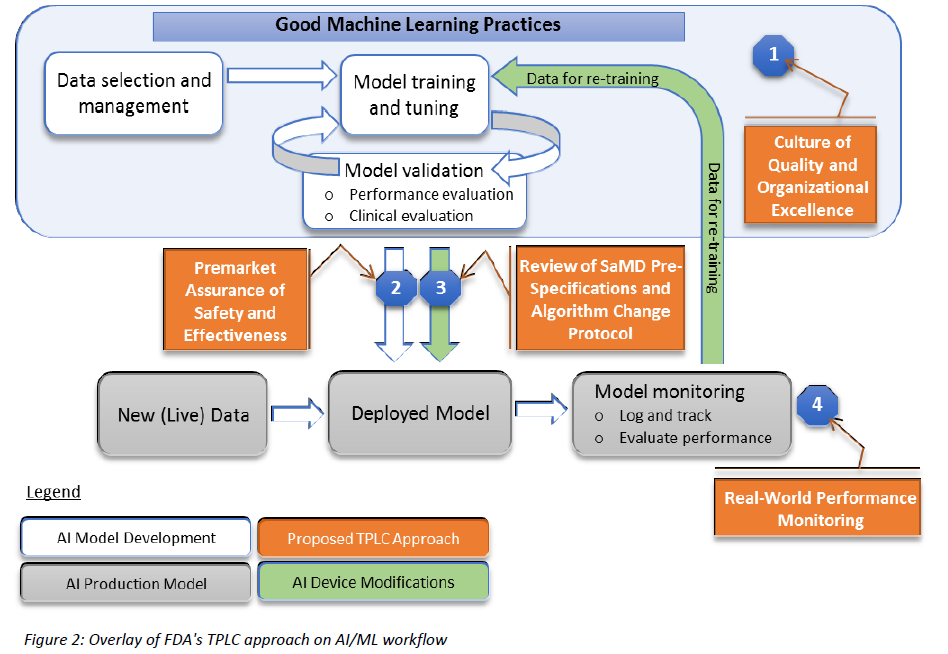
參考資料:“Proposed Regulatory Framework for Modifications to Artificial Intelligence/Machine Learning (AI/ML)-Based Software as a Medical Device (SaMD)-Discussion Paper”, p.8.
除上述重點外,就FDA於本項討論文件中所提,將自其他現有相關指引文件援引之某些重要機制,例如:GMLP、預定變更控制計畫(Predetermined Change Control Plan)等,亦有必要對其內涵稍加瞭解,現簡要整理於下:
(一)GMLP(於產品開發階段):
依討論文件內容,於此處所提到的GMLP,在概念上,其實是指那些與「優良軟體工程規範」(Good Software Engineering Practices)或「品質系統規範」(Quality System Practices)相類似之AI/ML之最佳範例(例如:數據資料管理、特徵值抽取、訓練與評估等),而其適用此類產品開發/製造之注意事項包括:
1. 現有可得之數據資料,對目前臨床實務問題之相關性;
2. 數據資料應要求具一致性、臨床相關性、可歸納性,且與 SaMD之預期用途與預定修改計畫相合致;
3. 用於訓練、調整與測試之數據集合(Datasets),應做適當區隔;及
4. 所輸出之資料與修改後演算法,均應具適當之透明度。
2. 數據資料應要求具一致性、臨床相關性、可歸納性,且與 SaMD之預期用途與預定修改計畫相合致;
3. 用於訓練、調整與測試之數據集合(Datasets),應做適當區隔;及
4. 所輸出之資料與修改後演算法,均應具適當之透明度。
(二)預定變更控制計畫(於上市前審查階段):
建議此類產品製造商,可在最初上市前審查期間內,選擇性提交「修改計畫」(Modification Plan),而FDA方面將會在一併考量其所提交之修改計畫是否可就其產品安全性與效用提供合理保證前提下,對該項SaMD產品之性能表現、及該製造商對演算法修改所產生風險之管控能力等項目,進行審查並作成決定。而根據FDA所作說明,就廠商對以AI/ML為基礎SaMD所為之修改之上市前安全性與功效管理,擬採納「預定變更控制計畫」此種方法,主要目的是希望確保開發廠商是在可控制對病患風險此情況下,執行此類演算法之變更(或修改),其主要包含下述幾項元素:
建議此類產品製造商,可在最初上市前審查期間內,選擇性提交「修改計畫」(Modification Plan),而FDA方面將會在一併考量其所提交之修改計畫是否可就其產品安全性與效用提供合理保證前提下,對該項SaMD產品之性能表現、及該製造商對演算法修改所產生風險之管控能力等項目,進行審查並作成決定。而根據FDA所作說明,就廠商對以AI/ML為基礎SaMD所為之修改之上市前安全性與功效管理,擬採納「預定變更控制計畫」此種方法,主要目的是希望確保開發廠商是在可控制對病患風險此情況下,執行此類演算法之變更(或修改),其主要包含下述幾項元素:
1. SaMD 預定規格(SaMD Pre-Specifications,簡稱SPS):SaMD產品之「功能表現」或「輸入資料類型」之預期性修改,與(或)對其「預期用途」所為之相關變更。而這些是製造商原定之規劃,亦即當使用 SaMD時將會實現之變更類型。 SPS圍繞該原始醫療器材最初規格與標籤前提下,預先繪製出其「潛在變更之區域」。(此即為製造商期望該演算法於使用/學習後成為「什麼」)
2. 演算法變更協定(Algorithm Change Protocol,簡稱ACP):SPS中所描述預期修改類型之風險而制訂之具體方法(如表一)。 ACP針對所依循之數據資料與流程做逐步描述,以便所作修改可達成目標,且該醫療器材於修改後仍可維持安全性與功效(此即為演算法「如何」能在邊學習及改變情況下,仍可同時保持其安全性與功效)。
3. 另外,FDA也預期,在某些情況下,經於真實世界使用與學習適應,修改後SaMD所具之風險或預期用途有可能會產生明顯之變化。而在此種情形下,就廠商原所提出之SPS與ACP建議方案,或有可能已不適於用來管理其產品對使用病患之風險,故建議製造商,宜就該項以AI/ML為基礎軟體使用後之修改所將對病患造成之風險來進行評估,且FDA亦將會視其所聲明之修改類型與潛在風險來決定應採取何種管理要求。
2. 演算法變更協定(Algorithm Change Protocol,簡稱ACP):SPS中所描述預期修改類型之風險而制訂之具體方法(如表一)。 ACP針對所依循之數據資料與流程做逐步描述,以便所作修改可達成目標,且該醫療器材於修改後仍可維持安全性與功效(此即為演算法「如何」能在邊學習及改變情況下,仍可同時保持其安全性與功效)。
3. 另外,FDA也預期,在某些情況下,經於真實世界使用與學習適應,修改後SaMD所具之風險或預期用途有可能會產生明顯之變化。而在此種情形下,就廠商原所提出之SPS與ACP建議方案,或有可能已不適於用來管理其產品對使用病患之風險,故建議製造商,宜就該項以AI/ML為基礎軟體使用後之修改所將對病患造成之風險來進行評估,且FDA亦將會視其所聲明之修改類型與潛在風險來決定應採取何種管理要求。
| 要素項目 | 內容 |
| 數據資料管理 |
|
| 再訓練 |
|
| 功能表現評估 |
|
| 更新升級程序 |
|
表一、ACP組成要素表
參考資料:“Proposed Regulatory Framework for Modifications to Artificial Intelligence/Machine Learning (AI/ML)-Based Software as a Medical Device (SaMD)-Discussion Paper”, p.11.
總的來說,人工智慧及機器學習軟體,基於其可從真實世界反饋中學習與改善其功能表現之能力,而具有可從根本上改變醫療照護服務之潛力,並正一步步地刺激、導引相關新興醫療器材之開發,不過…正如事物的一體兩面,此類包含以AI/ML技術為基礎之新興醫療器材產品,也將因其本身所具可不斷自我適應及修改之性質,改變了其原本之風險(或將超越其本身預期使用範圍)並進一步影響其安全性;因此,究如何為此類功能強大之新興醫療器材產品,形塑出一套合適之管理規範,一方面,是各國主管機關須妥善解決之問題,而另一方面,也一併牽動著其相關產業是否能真正在兼顧民眾健康安全此前提下快速發展並改善未來的醫療照護服務。此次美國FDA所提出之概念性管理架構,其後續之修正方向與將採之管理密度,對有意願(或正在)開發此類新興醫療器材產品(或軟體)之業者來說,頗值持續追蹤與關注。(依FDA方面所作說明,於完成針對其所提概念性管理架構之回饋意見收集後,下一階段將會綜整各界所提供之修正建議,草擬並正式發布一項新指引文件草案)
參考資料:
1. For more information about “Statement from FDA Commissioner Scott Gottlieb, M.D. on steps toward a new, tailored review framework for artificial intelligence-based medical devices”, please refer to this website:
https://www.fda.gov/news-events/press-announcements/statement-fda-commissioner-scott-gottlieb-md-steps-toward-new-tailored-review-framework-artificial
2. For more information about “FDA permits marketing of artificial intelligence-based device to detect certain diabetes-related eye problems”, please refer to this website:
https://www.fda.gov/news-events/press-announcements/fda-permits-marketing-artificial-intelligence-based-device-detect-certain-diabetes-related-eye
3. For more information about “FDA permits marketing of clinical decision support software for alerting providers of a potential stroke in patients”, please refer to this website:
https://www.fda.gov/news-events/press-announcements/fda-permits-marketing-clinical-decision-support-software-alerting-providers-potential-stroke
4. About the full text of the “Proposed Regulatory Framework for Modifications to Artificial Intelligence/Machine Learning (AI/ML)-Based Software as a Medical Device (SaMD) - Discussion Paper and Request for Feedback”, available at:
https://www.regulations.gov/document?D=FDA-2019-N-1185-0001
5. About the full text of the “Deciding When to Submit a 510(k) for a Software Change to an Existing Device”, available at:
https://www.fda.gov/media/99785/download
延伸閱讀:
-
2019-04-12
消息來源:


