【智財評析】保障境內民眾使用可負擔之新創學名藥品~歐盟執委會公布最新製藥業反競爭執法報告
2019-04-16 孫世昌 資深顧問

壹、歐盟執委會公布最新製藥業反競爭執法報告(2009-2017)
繼「歐盟執委會」(European Commission,以下簡稱執委會)於2009年對境內製藥業進行大規模反競爭調查後,此領域反競爭法令之執行與市場監督,已受到歐盟政府高度關注,而為避免病患對可負擔新創藥品之近用、新創醫療藥品開發、與國家健康照護系統支出成本,不會因「昂貴且不合理之藥價水準」、「製藥業者所採取之撤出(或不進入)市場進行競爭或其他商業策略」、「政府對藥品議價能力有限」等因素受不利影響,「歐洲理事會」(European Council)於2016年時,正式要求執委會研擬一份自其於2009年對製藥業進行反競爭調查(主要聚焦於逆向給付和解協議)後至目前為止之最新案件進度報告。基於前述原因,執委會已於今(2019)年1月28日,向歐洲理事會與議會(Parliament)同時提交了一份「2009-2017製藥業競爭法令執行調查報告(Competition Enforcement in the Pharmaceutical Sector, 2009-2017)」(即COM(2019) 17 final),除回應理事會與議會之要求外,併透過列舉實際裁罰案例,為歐洲藥品市場參與者提供導引協助其遵守相關法令規定,以維持良性競爭。而值得一提的是,我國亦於今年3月6日,由「衛生福利福部食品藥物管理署」及「公平交易委員會」會銜發布「西藥專利連結協議通報辦法」,明訂業者於依「藥事法」第48-19條第1項所規定書面通報內容範圍,涵蓋「涉及逆向給付利益」相關事項,正式將可能違反「公平交易法」之逆向給付和解協議納入管理。
貳、2008-2009年大規模反競爭調查
為讓讀者能較易掌握執委會反競爭執法報告,現先就執委會前於2009年對製藥業所進行之大規模反競爭調查過程(以逆向給付和解協議為主),稍作一簡單整理及回顧:
一、分析關鍵要件:指出所簽訂之和解協議必定包含如下兩關鍵要件:
(一)可預見學名藥商所開發新學名藥品之未來上市將因此而受有「限制」、
(二)可預見一項有價物未來將自原專利藥商移轉至學名藥商(此點為執委會將來判斷此類協議是否違反歐盟競爭法令之重要基準)。
二、區分受調查和解協議類型:
(一)採「限制」要件之分類:
- 最直接限制模式:即於和解協議中明確約定,除限制競爭學名藥商對原專利藥商所為之「專利無效」挑戰外,亦將限制該學名藥商所生產之學名藥,需待原專利藥品專利保護期限屆至後,方能上市(即所謂非競爭條款)
- 原專利藥商授權模式:指於取得原專利藥商許可前提下,允許其他學名藥商於市場上販售其所生產之專利藥品(此屬限制新學名藥品進入市場之一種模式,理由是競爭學名藥商將因簽訂前述和解協議,而不能按原規劃時程上市銷售其所開發之學名藥品);故於此模式下,競爭學名藥商所開發新學名藥品之上市時點,將受原專利藥商所控制。
- 其他相類似模式:即以相類似邏輯所達成之訴訟和解協議,並於協議中要求競爭學名藥商成為原專利藥商之藥品批發商,亦即要求學名藥商向原專利藥商採購主要活性成分來產製藥品(惟於此類協議中所可能存在之潛在限制性條款必須明確)。
- 直接金錢移轉:例如由原專利藥商給付學名藥商一大筆資金之情況,即屬最為明顯之有價物移轉案例。按和解協議中所擬定之約款,其金錢給付,可能採「合法」方式來「補償」學名藥商延遲其學名藥品上市時所將遭受之損失,或者購買某種有價資產(例如:競爭學名藥商股票)。(此作法背後之思維,即在延遲學名藥商所開發學名藥品之上市時點,透過持續販售原專利藥品,來做為維護原專利藥商既有市場利潤之方法)
- 其他型式之有價物移轉:包括簽訂各類型銷售同意書、或由原專利藥商約定給予競爭學名藥商一定商業利潤之附屬協議書(例如:允許其於原專利藥品專利保護期限屆至前,在其他區域銷售其他藥品)。
三、細緻化再分類(結合兩關鍵要件)
(一)A類型專利訴訟和解協議:此屬「未限制」學名藥商上市銷售其所開發學名藥品之協議類型,又稱為「平安脫身」和解協議(一般情況下此類協議「非屬」執委會所認須調查之協議類型)。
(二)B類型專利訴訟和解協議:此為學名藥商受有限制之協議類型,可再分為B.I.與B.II.兩次小類:
- B.I.類訴訟和解協議:即於協議中,明確對學名藥廠產品上市銷售時點作出限制(未包含任何形式有價物之移轉);
- B.II.類訴訟和解協議:即於協議中,可預見「某項有價物」(包含金錢或非金錢形式)自原專利藥商移轉至學名藥廠。(可參考附圖-1)
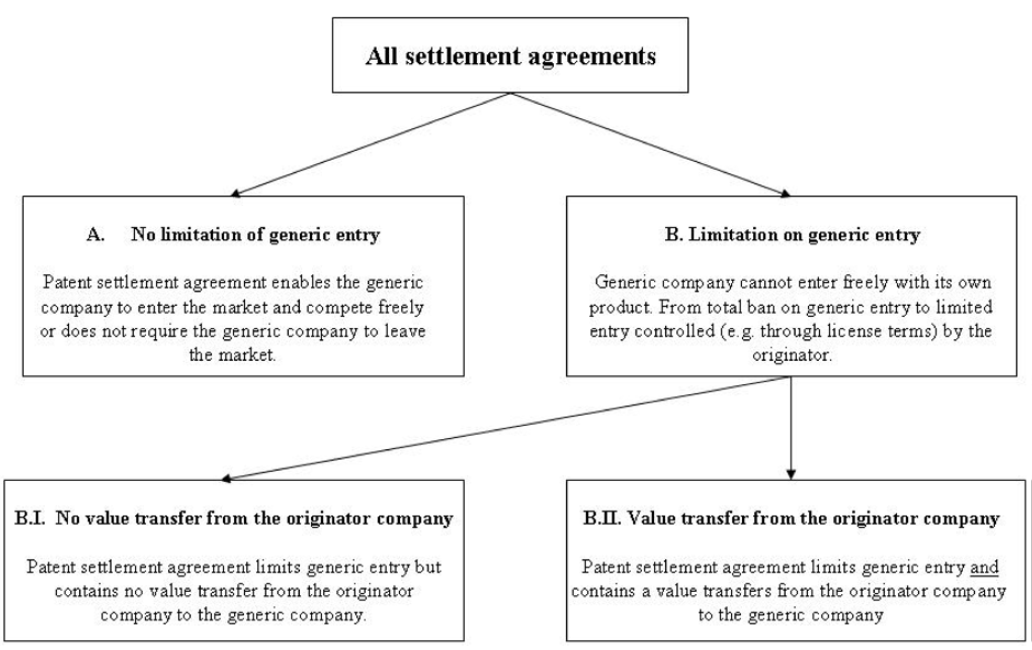
資料來源:“1st Report on the Monitoring of Patent Settlements(period: mid 2008 -end 2009)”, Published on July, 2010.
於完成大規模調查與評估後,執委會旋即發出正式聲明,表示將針對上述「B.II 類」案件,做更進一步之分析與調查,同時亦會持續就造成學名藥品上市遲延之逆向給付和解協議案件進行必要之監管。
參、歐盟製藥業反競爭執法報告重點摘要
承上,依上述聲明及回應理事會要求等前提下,執委會就其於2009-2017年間續行對境內製藥業反競爭案件進行之調查、執法與實際裁罰情況,以併採案例說明方式,彙整成一份製藥業反競爭執法報告,因內容涵蓋範圍十分廣泛,故現僅就與和解協議有關之反競爭實際執法狀況與裁罰案例部分,擇要說明如下:
一、揭示NCAs執法工具/使用頻率:
(一)未經宣布之實地查驗:即為收集涉嫌反競爭行為證據,而對公司所進行之實地突襲搜查,就未能提交檢查或阻止檢查者(例如:破壞檢查封印),將導致巨額罰款(實務上有近62%之調查有採此種方式)。
(二)資訊請求:此被認為是一種強大的調查工具,因業者在面臨將可能被罰款之情況下,多半會被迫提交出更完整及正確之資料(實務上有近90%之調查皆使用此項工具)。
(三)訪談(於近45%之調查過程中有進行訪談)。
二、實際調查狀況統計:
(一)指出於2009-2017年間,執委會與各會員國之「國家競爭主管機構」(National Competition Authorities,簡稱NCAs),就先前涉及反競爭問題之100多項案件,進行大量之調查工作(此未導致執委會做出干預之決定),而就目前正持續調查之案件中涉藥品者,共計20多件(如附圖-2)。
(二)於2009-2017年間受調查之對象包括:藥品製造商、批發商及零售商,所涉及藥物種類包括:用於化療之抗癌藥品、抗抑鬱藥、強效止痛藥、預防心臟衰竭藥品等。
附圖-2:NCAs對製藥業所為之反競爭調查(2009-2017)
.png)
資料來源:“Competition Enforcement in the Pharmaceutical Sector, 2009-2017(COM(2019) 17 final)”, Published on Jan, 2019.
(三)會導致NCAs作出干預決定之案件類型/比例如後:
- 濫用支配地位(佔45%);
- 簽訂限制性協議:包括競爭藥商間所簽訂之「限制性橫向協議」(例如:延遲給付協議,佔31%)、縱向協議(例如:禁止經銷商銷售競爭對手學名藥品)。
三、延遲給付和解協議重要案例(摘要)
依此份報告內容,點出延遲給付和解協議多半係因原專利藥商與學名藥商間專利訴訟糾紛而引發,惟於近年實務上,有心之市場參與者,似可透過採取其他商業策略遊走於法令灰色地帶進行安排,故現將ECAs已作成裁罰決定之重要案例摘要於下,俾利參考:
(一)Fentanyl 案:
- 原因:Sandoz公司與Johnson & Johnson子公司簽訂「共同促銷協議」(雙方約定以每月支付超過其所開發新學名藥品未來上市銷售利潤之金額,來做為Sandoz公司不進入荷蘭市場之對價)。
- 理由:依所發現內部文件顯示,Sandoz公司決定放棄進入市場,以交換一部分商業利潤,而原專利藥商一部分專屬利潤亦可因此而不受學名藥競爭影響(兩競爭對手未彼此競爭,而是同意共同朝以不將新學名藥品上市方式來保持原專利藥品當前之高價)。前述協議延遲新學名藥品進入市場期間達17個月之久,並人為地提高荷蘭當地Fentanyl藥品價格(此對當地病患及健康照護系統均造成不利影響)
- 結果:執委會認為雙方協議已違反TFEU第101條之限制性競爭,對Johnson & Johnson公司罰款1,080萬歐元,對Novartis公司罰款550萬歐元。(本案雙方均未提出上訴)
(二)Citalopram案
- 原因:Lundbeck公司與競爭學名藥商簽訂延遲Citalopram新學名藥品(一種抗抑鬱藥品)上市協議。
- 理由:依所調查協議內容,競爭學名藥商明確承諾不與Lundbeck公司競爭,而Lundbeck公司則向其支付大量金錢購買所開發之新學名藥品(目的只是單純地進行銷毀),並於協議中保障其銷售利潤。
- 結果:執委會於2013 年所出決定,依歐盟普通法院(General Court)於支持前述決定所為判決內容,此種延遲給付協議,實類似一種市場共享,已嚴重違反TFEU第101條規定,對丹麥製藥公司Lundbeck公司處以9,380萬歐元罰款,並對其他4家學名藥商處以5,220萬歐元罰款。
(三)Perindopril案
- 原因:Servier公司與數家競爭學名藥商簽訂專利訴訟和解協議以延遲Perindopril新學名藥品(一種降血壓藥品)之上市。
- 理由:依調查結果,Servier公司向數家競爭學名藥商支付數千萬歐元(包括收購競爭技術),目的在保護其暢銷藥Perindopril,免於來自歐盟境內學名藥之價格競爭。
- 結果:執委會於2014年作出決定,對法國Servier公司及5家學名藥商(Niche/Unichem、Matrix/Mylan、Teva、Krka與Lupin)處以總額4,277億歐元之罰款;至2018年12月12日,歐盟普通法院依第101條規定,確認執委會之調查結果(不包括Krka協議),但否定執委會所提Servier公司行為亦同時違反 TFEU 第102 條結論,故將罰款總額調降至3.15億歐元。(雙方仍可提出上訴)
除上述內容,執委會還於報告中強調,有鑑於反競爭案件之調查往往非常複雜且需大量資源,故各會員國NCAs均將反競爭調查重點,聚焦在那些可為市場參與者提供法令遵循指引及防止其從事類似行為之重要案件上,且認為,目前歐盟主管機關實務上所採警戒性反競爭審查,確有達到改善藥品市場不當競爭之目的,而更重要的是,在以2009年對歐洲製藥業所進行之全面性反競爭調查為重要基礎及各會員國NCAs緊密合作等前提下,透過實際執法,已漸為歐盟競爭法在藥品市場之應用,奠定不少開創性案例(部分案例如上文整理)。
肆、值留意處
綜上,透過觀察歐盟製藥業反競爭執法現況,似有如後幾點值得留意:其一,對主管機關來說,基於製藥業本身特性,就市場參與者所採之商業競爭模式,正隨產業發展而趨複雜且更多變化,故對業者實務上所採遊走於法令灰色地帶之市場商業競爭策略,其違法要件與類型化判斷,皆是未來各國於製藥業反競爭執法上所需面對之挑戰;其二,對業者來說,於主管機關尚未明確化違法類型前,該如何判斷自身所採市場競爭策略是否已牴觸法令?有無任何規則可資依循?這或多或少也將增加將來於法令遵循上之困難度;其三,對身處仰賴與歐、美等先進國家進行貿易為主國家之業者而言,參考美、歐政府對此類案件所採類型化判斷要件及違法案例,均有助於降低未來法令遵循上之風險。
參考資料:
- For more information about the news “Competition: Commission report finds active competition enforcement contributes to affordable and innovative medicines”, please refer to this website:http://europa.eu/rapid/press-release_IP-19-741_en.htm
- About the “Report on Competition enforcement in the pharmaceutical sector (2009-2017)”, please refer to this website:http://ec.europa.eu/competition/sectors/pharmaceuticals/report2019/index.html
- About the “1st Report on the Monitoring of Patent Settlements (period: mid 2008 - end 2009)” , please refer to the website:http://ec.europa.eu/competition/sectors/pharmaceuticals/inquiry/patent_settlements_report1.pdf
- 有關「西藥專利連結協議通報辦法」,可參考網站:https://gazette.nat.gov.tw/egFront/detail.do?metaid=105368&log=detailLog
- 有關美國FTC對於逆向給付和解協議分類及新近規範狀況,可參考本所網站文章:http://www.giant-group.com.tw/law-detail-706.html
延伸閱讀:
-
2019-04-12
-
2019-03-15
-
2019-03-13
消息來源:


